










研究目的:本试验采用听诊式参考血压计通过同臂顺序测量法进行临床研究。受试者的同一手臂依次使用参考血压计和试验产品进行测量,记录听诊法和试验产品的数据并进行统计,评价试验产品血压的准确度。
病例数:根据ISO 81060-2:2018+Amd 1:2020的要求,采用听诊式参考血压计进行血压准确度临床研究,计划纳入至少85名受试者,包括35名3-12岁的儿童和50名12岁以上的受试者。其中至少30%的受试者应为男性,30%的受试者应为女性。所有受试者分别在常压环境和高压空气舱内进行血压准确度临床研究。
入选标准:
① 年龄≥18岁,男女不限;
② 22cm≤上臂周长≤36cm;
③ 受试者自愿参加该研究并能够遵循研究步骤;
④ 受试者本人或由合法授权代表签署知情同意书。
排除标准:
① 患镰状细胞疾病和任何有皮肤损害或预期会发生损害的患者;
② 有严重的凝血机制障碍的患者;
③ 患有严重心脏疾病(包括明显心律不齐、心动过速、孤立性室性早搏(VPB)、心房颤动)、肝肾疾病或血液循环障碍的患者;
④ 在手臂测量部位存在外伤以及皮肤溃疡的患者;
⑤ 正在进行血管内的介入或治疗、或动-静脉(A-V)分流的患者;
⑥ 研究者认为因其他原因不适宜参加本次临床研究者。
试验流程:
1. 受试者准备
(1)尽可能让受试者坐在舒适的位置,双腿不要交叉,双脚平放在地板上;
(2)受测者的背部、肘部和前臂有支撑;
(3)测量部位与左心室水平;
(4)受测者应尽可能放松;在整个过程中,受测者应避免说话;
(5)应在裸臂上使用袖带,且袖带近端不得压迫手臂;
(6)在测量第一个参考读数之前,应等待5分钟。
2. 观察员准备
(1)观察员应接受培训,掌握使用公认的临床血压测量规程进行静息血压读数的正确方法;
(2)观察员在进行血压读数时应进行充分的练习;
(3)每个观察者对参考血压计的观察记录不得让其他观察者看到;
(4)上述任何一名观察者均不得看到试验设备的测定结果,由第三名观察员记录被测血压计的测定结果,利用电子装置记录被测血压计的测定结果;
(5)观察员应使用Korotkoff声[第五相(K5)]来确定参考舒张压;
(6)如果无法听到用于确定参考舒张压的Korotkoff声[第五相(K5)],则应排除受试者。
3. 参考读数
(1)两名观察员应使用双头听诊器同时测定每名受试者的收缩压和舒张压;
(2)除非被测血压计适用于心律明显异常的情形,否则如果任一名观察员发现明显异常的心律,应排除该读数;
(3)任何一对观察员的收缩压值或舒张压值相差超过4mmHg(0.53kPa)的情况都应排除在外;
(4)在读取一组成对测试参考值后,应检查观察员之间的差异;如果任何读数被排除在外,应额外读取一对读数,以确保有效测试参考值的对数达到要求。每名受试者最多读取8对读数。
4. 试验方法
选择同臂顺序测量法:
(1)记录受试者的身份、年龄、性别、身高和体重、受试手臂的臂围;
(2)测试前让受试者安静地坐至少五分钟;
(3)两名观察员应同时使用参考血压计测量受试者的血压并记录血压测量结果(注:两名观察员不可查看对方的测量记录)。同时,试验血压计观察员需计算参考血压测量值之间的差值,并计算平均脉率。如发现在同一组中通过双听诊器测量的收缩压值或舒张压值之差超过4mmHg(0.53kPa),试验血压计观察员应提示此测量数据不被采用且需重新测量;
(4)等待60秒;
(5)在受试者的同一测试臂上测定血压(由研究设备测定)。利用电子手段记录研究设备的测定结果;
(6)清除研究设备上一次测定的记忆,然后至少等待60秒;
(7)在计算准确度时不要使用(3)和(5)中获得的数据;
(8)两名观察员应同时使用参考血压计测量受试者的血压并记录血压测量结果(注:两名观察员不可查看对方的测量记录)。同时,试验血压计观察员需计算参考血压测量值之间的差值,并计算平均脉率。如发现在同一组中通过双听诊器测量的收缩压值或舒张压值之差超过4mmHg(0.53kPa),试验血压计观察员应提示此测量数据不被采用且需重新测量。
(9)等待60秒。
(10)在受试者的同一测试手臂上测定血压和脉搏(由研究设备测定血压1和脉率1 )。利用电子手段记录研究设备的测定结果。
(11)等待60秒。
(12)两名观察员应同时使用参考血压计测量受试者的血压并记录血压测量结果(注:两名观察员不可查看对方的测量记录)。同时,试验血压计观察员需计算参考血压测量值之间的差值,并计算平均脉率。如发现在同一组中通过双听诊器测量的收缩压值或舒张压值之差超过4mmHg(0.53kPa),试验血压计观察员应提示此测量数据不被采用且需重新测量。
(13)等待60秒。
(14)如果有以下情况,应排除来自受试者的所有数据:任何两个参考收缩压值的差异超过12mmHg(1.60kPa);或任何两个参考舒张压值的差异超过8mmHg(1.07 kPa)。
(15)对每个受试者重复上述(10)至(13)步骤,直到完成所需数量的有效参考读数和测定读数,如有排除数据,则需重新测量,每个受试者最多采集8对读数。
评价指标:
1. 有效性评价标准
试验产品应满足以下两个标准:
(1)对于所有受试者,试验产品的n个测定值与对应参考血压计读数分别按收缩压和舒张压计算差值,差值的平均值不得超过±5.0mmHg(±0.67kPa),且差值的标准差小于8.0mmHg(1.07kPa)。
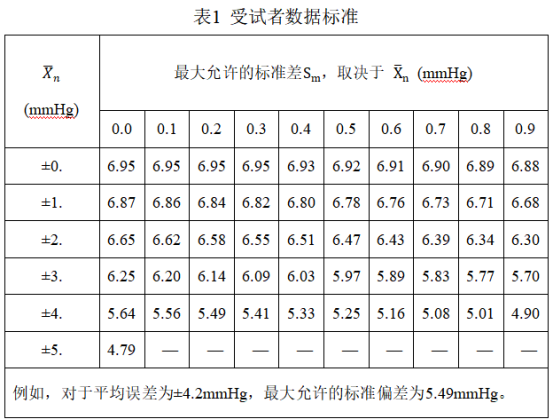
(2)对于m名受试者的每一对收缩压和舒张压,每个受试者的试验产品测量值和对应参考血压计读数的标准差应符合表1中所列的标准。
2. 按臂围显示所有受试者结果的散点图
按臂围显示所有受试者结果的散点图,其中Y轴为试验产品血压值和参考血压值之间的差值,X轴为受试者的臂围,同时还应以垂直线标明袖带范围的边界。散点图应分收缩压和舒张压两项。
3. 安全性指标
(1)不良事件
不良事件包括:与器械相关的不良事件(如测量部位短暂的红肿、瘙痒、麻痹、血肿、淤点等);
严重不良事件是指临床研究过程中发生的导致死亡或者健康状况严重恶化,包括:致命的疾病或者伤害;身体结构或者身体功能的永久性缺陷;需要住院治疗或者延长住院时间;需要采取医疗措施以避免对身体结构或者身体功能造成永久性缺陷等。
(2)生命体征(体温、脉搏、呼吸、血压)。
(3)器械缺陷发生率:器械缺陷发生率=器械缺陷发生次数/总次数×100%。

电话:15838027610
地址:四川省成都市武侯区武侯大道铁佛段1号1栋2单元9层916号
