










试验目的:本临床试验采用前瞻性、多中心、非盲、随机、平行对照、非劣效临床试验设计方法,以已上市的软性亲水接触镜为对照产品,评价试验产品(软性亲水接触镜)用于矫正近视性屈光不正的有效性和安全性。
病例数:根据国家药品监督管理局医疗器械技术审评中心发布《软性接触镜临床评价注册审查指导原则》(2018年第18号)中“(五)临床试验样本量”的要求,临床试验最终完成总样本量不少于120例,非劣效界值不大于10%,试验组不少于60例。同时根据《医疗器械临床试验设计指导原则》中样本量估算方式进行以下样本量计算。
本次临床试验采用前瞻性、多中心、非盲、平行对照的试验设计方法,采用试验产品与已上市同类产品进行比较研究的方法,根据临床需求及产品特性,主要从有效性角度作非劣效性试验,要求允许的二类误差概率不超过β,同时,考虑到产品临床试验中的主要有效性评价指标为产品临床使用有效率,故样本量的计算公式为:
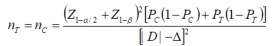
式中:nT、nC分别为试验组和对照组的样本量;Z1-α/2、Z1-β为标准正态分布的分数位,当显著性水平α为0.05时,双侧检验,Z1-α/2=1.96,当β=0.2时,Z1-β=0.842。PT、PC分别为试验组和对照组临床使用有效率;|D|为两组预期率差的绝对值,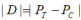 ,∆为非劣效界值,取负值。参考既往临床试验数据,配戴软性亲水接触镜的有效率约为96%。参考以上数据,预估对照组有效率为96%,即PC为96%,假设试验组的预期有效率与对照组一致均为96%,即PT=PC=96%。预期试验组产品与对照产品的临床使用有效率的率差值在10%以内,则认为两组疗效相当(即:非劣性界值∆为-10%),代入公式:
,∆为非劣效界值,取负值。参考既往临床试验数据,配戴软性亲水接触镜的有效率约为96%。参考以上数据,预估对照组有效率为96%,即PC为96%,假设试验组的预期有效率与对照组一致均为96%,即PT=PC=96%。预期试验组产品与对照产品的临床使用有效率的率差值在10%以内,则认为两组疗效相当(即:非劣性界值∆为-10%),代入公式:
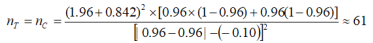
根据以上估算,总样本例数约为122例(试验组和对照组均不少于61例)。考虑20%脱落剔除率,本研究计划入组受试者152例。
入选标准:
(1)18≤年龄≤40岁,性别不限;
(2)受试者应分别检查两眼,框架镜最佳矫正视力均能达到5.0;
(3)配戴软性亲水接触镜范围在-1.00D~-8.00D之内(含-1.00D和-8.00D),主觉验光散光度数在-0.75D以下(含 -0.75D),球柱比≥3:1;
(4)受试者知情并自愿签署知情同意书。
排除标准
(1)单眼符合纳入标准;
(2)角膜平坦曲率未在39.00D~48.00D之间;
(3)受试者正在使用可能干扰接触镜配戴的局部眼科药物或全身药物(三环类抑郁药、吩噻嗪类、全身麻醉药、免疫调节剂);
(4)受试者3个月内患有眼部疾病如眼部急性或慢性炎症、青光眼、角膜知觉异常、角膜上皮缺损、角膜内皮细胞减少、角膜损害等经眼科医生判断不能配戴者;
(5)受试者患有可能影响眼部的全身性疾病,经眼科医生判断不能配戴;
(6)参与本次试验前三个月内的任意一只眼睛曾受过眼外伤,包括但不限于眼前节挫伤、眼后节挫伤、开放性眼穿通伤、眼内异物、视神经挫伤、眼化学性烧伤等,以及经研究者判定可能会对临床试验结果造成影响的眼附属器损伤;
(7)受试者双眼任一眼压>21mmHg 或<10mmHg,或双眼眼压差>5mmHg;
(8)裂隙灯检查有以下检查结果:1)中重度干眼症(裂隙灯显微镜下检查存在多个象限角膜损伤或角膜荧光素钠染色点≥5个或泪膜破裂时间[Tear film Break-up Time TBUT]≤5s(检查标准见附件2);2)翼状胬肉;3)角膜视轴内瘢痕;
(9)角膜和结膜观察有以下任一情况的:a)睫状充血、球结膜充血、睑结膜观察、角膜新生血管形成等任一检查结果达到2级及以上的受试者;b)角膜上皮水肿、角膜基质水肿、角膜上皮微囊、角膜浸润等任一检查结果达到1级及以上的受试者;c)角膜检查发现下列任一情况的受试者如角膜糜烂、周边角膜溃疡、感染性角膜溃疡;d)眼部常规检查出现下列任一部位异常的受试者(眼睑、睑缘、泪膜、前房、虹膜、瞳孔、晶状体、眼底)(角膜及结膜的观察标准见附件3);e)角膜内皮多形性变化检查结果达到4级的受试者;
(10)受试者对接触镜材料或相关护理产品过敏;
(11)受试者配戴接触镜发生过严重并发症;
(12)受试者既往接受过角膜手术或眼内手术;
(13)30天内配戴过角膜塑形镜的受试者;
(14)3个月内参加过药物临床试验或1个月内参加过其他医疗器械临床试验的受试者;
(15)孕妇、哺乳期或半年内计划怀孕者;
(16)受试者生活或工作环境不适宜配戴软性接触镜,例如空气中弥散粉尘、药品、气雾剂(如发胶、挥发性化学物)、灰尘等;
(17)经研究者判断不适合参与本研究的其他情况。
临床评价标准:
(1)有效性评价指标
主要有效性评价指标:以戴镜有效率作为主要评价指标,评估试验产品的有效性。
有效标准:戴镜一周时分别检查两眼矫正视力均大于等于5.0(标准对数视力表)为“有效”。
戴镜有效率=达到有效标准的人数/总人数×100%。
次要有效性评价指标:以框架镜最佳矫正视力、接触镜矫正视力(视力检查使用标准对数视力表检查受试者的框架镜最佳矫正视力和接触镜矫正视力(远用)作为次要评价指标。
(2)安全性评价指标
主要安全性评价指标:以眼科常规检查、镜片配适状态、作为主要评价指标,评价产品的安全性。
眼科常规检查:裸眼视力(远用)、眼睑、睑缘、泪膜、结膜、角膜、前房、虹膜、瞳孔、晶状体、眼底、眼压等。
镜片配适状态:初次配戴及定期随访中需观察镜片在眼表的位置(中心定位)、覆盖度、松紧度、活动度,并评价和记录其等级。
次要安全性评价指标:以镜片状态、屈光状态、受试者可接受程度、产品润滑液情况作为次要评价指标,评价产品的安全性。
镜片状态:在定期随访中观察镜片的污损情况如:湿润度、沉淀、变形、变色、锈斑、划痕、破损等。
屈光状态:屈光度和角膜曲率,分别记录受试者戴镜前、后的屈光度变化(球镜度及柱镜度)和角膜曲率变化。
受试者可接受程度:舒适度、视觉、可操作性。
润滑液情况(包括产品外观,物理性状,润滑液性状)。

电话:15838027610
地址:四川省成都市武侯区武侯大道铁佛段1号1栋2单元9层916号
