










试验目的:本临床试验采用多中心、盲法、观察性研究的临床试验设计方法,以已上市的同类产品为对比试剂,评估考核试剂和对比试剂对同一受试者血浆样本中人磷酸化Tau-181蛋白(pTau-181)的含量检测结果的相关性、一致性。
病例数:根据EP9-A2要求,相关系数不小于0.975为目标值(r0)。预期本试验的考核试剂与对比试剂的相关系数为0.983(r1)。根据检验水准α=0.05(双侧),把握度1-β=0.8,计算样本量应入选210例。结合以往类产品临床研究的经验,考虑约5%的脱落率,本试验计划入组222例。
入选标准:
(1)性别、年龄不限;
(2)临床基本信息完整者,包括年龄、性别、临床诊断信息等;
(3)已确诊患有阿尔茨海默症或疑似患有阿尔茨海默症的患者;
(4)受试者或其法定监护人知情并签署知情同意书者。
排除标准:
(1)样本采集、处理和保存操作不符合说明书要求的;
(2)临床信息缺失者;
(3)未签署知情同意书者;
(4)研究者判断不适合入组者。
临床评价指标:
考核试剂与对比试剂检测结果的一致性分析
(1)分别以考核试剂检测结果、对比试剂检测结果为Y轴、X轴做散点图,拟合分析,计算回归方程截距、斜率及其95%置信区间,列出线性回归方程式求出相关系数(r),要求r应≥0.975;
(2)采用Bland-Altman法评价考核试剂与对比试剂检测结果的一致性,要求样本测量差值、比值落在95%一致性界限外点的比例在5%之内。
(3)医学决定水平处的预期偏倚及其可信区间
将医学决定水平预期偏倚的可信区间与允许误差的限值相比较(参照1/2CLIA’88、1/2来源于生物变异的总允许误差、1/2室间质评可接受范围、卫生行业标准等相关要求设定允许误差),如预期偏倚可信区间未超出相关允差限值,判定两检测系统等效,如未达到该标准,两检测系统不等效,需进一步改进方法进行临床验证。
1)对于任何给定的X值,Y的估计值
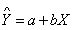
2)在给定的医学决定水平XC处的预期偏倚(BC)的估计值,按以下公式计算:
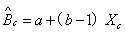
3)BC的95%可信区间(在XC处的真正偏倚)按以下公式计算:

其中估计值的标准误的计算公式如下:
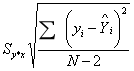

电话:15838027610
地址:四川省成都市武侯区武侯大道铁佛段1号1栋2单元9层916号
